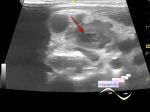
Трудности диагностики образований мочевого пузыря у детей
Метки: Последние публикации, УЗИ мочевого пузыря, дайджест, новости, онкология, урология
Содержание:
- Мезенхимальные новообразования
- рабдомиосаркома
- Воспалительные миелофибробластические опухоли
- лейомиома
- нейрофиброма
- Сосудистые аномалии
- Уротелиальные новообразования
- Уротелиальная карцинома
- Папиллярное уротелиальное новообразование с низким злокачественным потенциалом
- Уротелиальная папиллома
- Фиброэпителиальный полип
- Нейроэндокринные опухоли: Параганглиома
- Железистые опухоли мочевого пузыря: нефрогенная аденома
- Подводные камни визуализации
- Образование малого таза ошибочно принятое за образование мочевого пузыря
- Нормальный вариант или складка стенки мочевого пузыря ошибочно интерпретируемая как образование
- Воспалительное или неопухолевое образование, ошибочно истолкованное как опухоль
- Подвижный или ятрогенный материал в мочевом пузыре ошибочно интерпретируемый как опухоль
- Вывод
По данным публикации в журнале Радиографика (RadioGraphics) за октябрь 2017: Pearls and Pitfalls in Diagnosing Pediatric Urinary Bladder Masses / Жемчужины и подводные камни в диагностике образований мочевого пузыря у детей - внешняя ссылка
Опухоли мочевого пузыря у детей встречаются редко, а связанные с ними гистологические особенности и прогнозы отличаются от таковых у взрослых. У большинства детей с новообразованиями мочевого пузыря проявляются симптомы со стороны нижних мочевыводящих путей, которые могут включать гематурию, дизурию, частое мочеиспускание и императивные позывы к мочеиспусканию. Тем не менее, некоторые из этих новообразований могут быть идентифицированы случайно или сопровождаться общими симптомами, такими как вздутие живота. В целом, опухоли мочевого пузыря у детей можно разделить на те, которые происходят из эпителия мочевого пузыря, известные как уротелиальные новообразования, и мезенхимальные новообразования мочевого пузыря, которые встречаются чаще. Наиболее частым злокачественным новообразованием мочевого пузыря у детей является рабдомиосаркома, тогда как наиболее частым доброкачественным поражением мочевого пузыря в педиатрической популяции является папиллярное уротелиальное новообразование с низким злокачественным потенциалом (PUNLMP). Инструментом визуализации первой линии для оценки образований мочевого пузыря является ультразвуковое исследование, за которым может следовать компьютерная или магнитно-резонансная томография, если происхождение образования неясно или если подозревается отдаленное распространение. Хотя визуализация может позволить радиологу предложить дифференциальный диагноз на основе локализации образования и возраста пациента, обычно требуется биопсия ткани для установления точного диагноза. Она обычно выполняется при цистоскопии и может являться методом лечения в случаях, когда образование имеет небольшой размер и низкий потенциал рецидива. Знание клинических, гистопатологических и визуализационных особенностей распространенных новообразований мочевого пузыря имеет важное значение, поскольку оно может помочь в предотвращении ошибок визуализации. Они могут включать в себя неправильную интерпретацию новообразования в малом тазу как возникающего из мочевого пузыря или образования в мочевом пузыре как возникающего из органов малого таза, а также интерпретацию воспалительного образования или взвеси мочевого пузыря как новообразования.
Мезенхимальные новообразования
Рабдомиосаркомы являются наиболее распространенными злокачественными опухолями мочевого пузыря у детей младше 10 лет и составляют 5% всех солидных раков у детей. Хотя рабдомиосаркомы могут возникать в любом части тела, где есть примитивные мышечные клетки, примерно в 20% случаев они локализуются в мочевом пузыре и предстательной железе. Рабдомиосаркомы мочевого пузыря и предстательной железы имеют бимодальное возрастное распределение, при этом пик заболеваемости приходится на первые 2 года жизни, а другой пик приходится на подростковый возраст. Большинство рабдомиосарком возникают спорадически; однако некоторые генетические синдромы, такие как раковый синдром Ли-Фраумени(Li-Fraumeni), нейрофиброматоз 1 типа и множественная эндокринная неоплазия 2А типа, могут предрасполагать человека к развитию этой опухоли. Приблизительно у 10–20% пациентов с рабдомиосаркомой (независимо от локализации) на момент постановки диагноза обнаруживаются метастазы. Метастазирование обычно происходит в легкие, корковый слой костей и/или регионарные лимфатические узлы, при этом частота и характер заболевания различаются в зависимости от локализации и гистологических особенностей опухоли.
Гистопатологические подтипы рабдомиосаркомы включают эмбриональную рабдомиосаркому, которая составляет более 90% случаев и включает ботриоидные и варианты веретенообразных клеток, а также более редкие, более агрессивные альвеолярные и недифференцированные типы саркомы. Макроскопически эти опухоли обычно полиповидные, студенистые и многодольчатые. Микроскопически эмбриональный подтип состоит из мелких, темных, веретенообразных или округлых клеток с минимальной цитоплазмой, смешанных с различным количеством клеток, напоминающих рабдомиопласты. Альвеолярный подтип имеет тонкие фиброваскулярные перегородки, которые напоминают альвеолярные воздушные пространства и выстланы одним слоем кубовидных опухолевых клеток с гиперхромными ядрами.
Стратификация риска рабдомиосаркомы сложна и основана на системе стадирования TNM до лечения и системе клинической группировки после биопсии и резекции, установленной Межгрупповой группой по изучению рабдомиосаркомы (IRSG), которая была включена в Комитет группы детской онкологии по саркоме мягких тканей. Информация из обеих этих систем учитывается для присвоения пациенту уровня риска (низкий, средний или высокий). Система стадирования IRSG основана на размере (<= 5 см или > 5 см), инвазивности (т. е. локализована ли опухоль в анатомическом месте происхождения) и узловом статусе (т. е. вовлечены ли региональные лимфоузлы, по данным гистологического анализа) опухоли и места первичного рака (классифицированного как неблагоприятное анатомическое место для опухолей, исходящих из мочевого пузыря и предстательной железы). На исход влияют возраст пациента и подтип опухоли. Лица моложе 1 года и лица в возрасте 10 лет и старше чувствуют себя хуже; 51-53% лиц в этих возрастных группах по сравнению с 71% лиц в возрасте 1-9 лет имеют 5-летнюю бессобытийную выживаемость. Эмбриональный гистопатологический подтип рабдомиосаркомы связан с 82% 5-летней бессобытийной выживаемостью по сравнению с альвеолярным подтипом, который связан с 65% 5-летней бессобытийной выживаемостью.
С учетом стратификации риска для официальной визуализации и определения стадии рабдомиосаркомы необходимы КТ грудной клетки, КТ или МРТ малого таза и регионарных лимфатических узлов, сцинтиграфия костей и, возможно, аспирация костного мозга. Кроме того, появляется все больше данных, подтверждающих использование функциональной визуализации с помощью позитронно-эмиссионной томографии (ПЭТ) с фтор-18-фтордезоксиглюкозой для обследования и стадирования, особенно для выявления отдаленных метастазов и мониторинга ответа на лечение.
На эхограммах рабдомиосаркомы мочевого пузыря обычно большие и узловатые, часто связаны с обструкцией мочевыводящих путей, обычно имеют четкий контур, слегка гипоэхогенны и гомогенны. Ботриоидный подтип рабдомиосаркомы может иметь вид грозди винограда. Эти опухоли обычно локализуются в области пузырного треугольника и шейки мочевого пузыря. На КТ-изображениях опухоли обычно имеет неоднородное затухание, но в целом меньшее затухание по сравнению с нормальной мышечной тканью. При МРТ новообразование обычно имеет равномерную низкую интенсивность сигнала на Т1-взвешенных изображениях и неоднородную высокую интенсивность сигнала на Т2-взвешенных и контрастно-усиленных Т1-взвешенных жиронасыщенных изображениях. Более равномерная низкая интенсивность сигнала на Т1-взвешенных МР-изображениях в основном обусловлена областями с некротической тканью с низкой интенсивностью сигнала, которые легче различить на Т2-взвешенных и контрастно-усиленных МР-изображениях. Хотя неэмбриональные подтипы рабдомиосаркомы более агрессивны, исследование с участием 14 детей с рабдомиосаркомой не выявило убедительных доказательств особенностей томографической визуализации, которые могли бы помочь предсказать подтип опухоли.
Хемотерапия обычно является первой линией лечения рабдомиосаркомы перед операцией или лучевой терапией. В большой международной серии, включающей пациентов, получавших лечение по поводу рабдомиосаркомы мочевого пузыря, 78 (48%) из 164 пациентов были вылечены с помощью химиотерапии, 49 (30%) пациентам потребовалась частичная цистэктомия, а 34 (21%) из них подверглись полной цистэктомии. Пациенты с отсутствием прогрессирующего или остаточного заболевания после завершения терапии обычно находятся под наблюдением с визуализацией в течение не менее 5 лет для мониторинга возможного рецидива. Опухоль рецидивирует примерно у 30% пациентов, причем 95% рецидивов возникают в течение 3 лет после начала терапии. Пациенты с метастатическим заболеванием имеют гораздо худшие результаты, особенно при поражении кортикального слоя кости или костного мозга. От 14% до 16% этих пациентов имеют 3-летнюю бессобытийную выживаемость по сравнению с общей 3-летней бессобытийной выживаемостью примерно 30%.
Воспалительные миелофибробластические опухоли
Воспалительные миелофибробластические опухоли (IMT) ранее были описаны в литературе под разными названиями, включая псевдосаркоматозную опухоль, веретеноклеточную опухоль и атипичную фибромиксоидную опухоль. Хотя эти опухоли могут возникать в различных местах, их локализация в мочевом пузыре встречается редко, и эти опухоли считаются доброкачественными. Приблизительно 25% всех IMT мочевого пузыря манифестируют у детей со средним возрастом около 7 лет. Наиболее распространенные симптомы при манифестации включают гематурию и боль в животе.
Макроскопически IMT выглядят как полипоидные, бледные, плотные образования с поверхностными изъязвлениями. Микроскопически они состоят из веретенообразных клеток в миксоидной строме с рассеянными хроническими воспалительными клетками. Хотя их причина неясна, некоторые эксперты предполагают инфекционный или травматический процесс из-за присутствия воспалительных клеток.
При визуализации IMT обычно видны в куполе мочевого пузыря. При проявлении они могут быть большими, вероятно, из-за своего расположения и медленного роста, со средним размером 5,5 см; однако их размер может варьироваться от 1,8 до 13,0 см. Поскольку эти опухоли могут выглядеть так же, как рабдомиосаркомы, окончательный диагноз нельзя поставить только с помощью радиологического исследования; требуется биопсия тканей. Даже при диагнозе, основанном на биопсии, клеточные особенности IMT могут имитировать признаки злокачественной веретеноклеточной опухоли, и может быть полезным тестирование на белок киназы анапластической лимфомы, поскольку это наблюдается примерно в 33–89% случаев ИМТ.
Хотя известно, что локальный рецидив опухоли возникает после резекции IMT у взрослых, биологическое поведение IMT мочевого пузыря у детей неизвестно. Исследователи в одном из исследований проанализировали 42 случая IMT мочевого пузыря у детей и не обнаружили опубликованных статей, описывающих локальные рецидивы или метастатическое поражение в педиатрической популяции.
Лейомиомы мочевого пузыря встречаются редко, составляя 0,43% всех подтипов мезенхимальных опухолей мочевого пузыря; насколько это известно, на сегодняшний день есть только два опубликованных отчета о случаях с участием детей. Общие проявления лейомиомы мочевого пузыря включают обструкцию мочевыводящих путей, частое мочеиспускание, дизурию и гематурию. Эти опухоли чаще встречаются у женщин в возрасте 30–60 лет.
По локализации лейомиомы мочевого пузыря могут быть эндовезикальными (в 86% случаев), интрамуральными (в 11% случаев) или экстравезикальными (в 11% случаев), при этом эндовезикальный подтип чаще всего вызывает симптомы обструктивного мочеиспускания. Визуализационные характеристики этих опухолей очень похожи на таковые для миомы матки: обычно одиночное, гомогенно ослабляющее солидное образование с переменными характеристиками усиления при поперечном изображении, с интенсивностью сигнала от средней до низкой на Т1- и Т2-взвешенных МР-изображениях. Однако для подтверждения диагноза и исключения лейомиосаркомы необходим гистопатологический анализ. Способом лечения является иссечение опухоли, без риска рецидива или распространения.
Доброкачественные опухоли оболочек нервов редко встречаются в мочевом пузыре, но когда они все же встречаются, они обычно имеют плексиформную форму. Приблизительно 63–75% нейрофибром мочевого пузыря выявляют у пациентов моложе 18 лет, причем мочевой пузырь является наиболее частой локализацией нейрофибром, поражающих мочеполовую систему. Они поражают как спинномозговые нервы, так и вегетативные нервы стенки мочевого пузыря, хотя способность к мочеиспусканию не обязательно может быть нарушена, а в некоторых случаях болезнь может протекать бессимптомно. Результаты визуализации мочевого пузыря могут быть первым проявлением нейрофиброматоза 1 типа, и, следовательно, знание основного синдрома не всегда является обязательным условием для постановки диагноза, хотя можно выявить кожные стигмы синдрома во время выполнения УЗИ или из описания клиницистом клинического осмотра.
При визуализации нейрофиброма выглядит как солидное образование и может проявляться очаговым поражением или диффузным утолщением стенки мочевого пузыря. На МРТ эти опухоли обычно имеют однородную низкую интенсивность сигнала на Т1-взвешенных изображениях и высокую интенсивность сигнала на Т2-взвешенных изображениях. На Т2-взвешенных МР-изображениях плексиформные нейрофибромы часто проявляют признаки мишени с высокой интенсивностью сигнала на периферии и меньшей интенсивностью сигнала в центре. Дифференциальный диагноз включает рабдомиосаркому и ганглионеврому. Несмотря на то, что резекция опухоли может облегчить симптомы масс-эффекта, вызываемого нейрофибромой, тотальная резекция затруднена, поскольку большинство этих опухолей имеют плексиформную форму. Существует риск злокачественного перерождения нейрофибромы; однако в серии случаев с участием четырех детей с нейрофибромой мочевого пузыря не было обнаружено, что у этих пациентов развилась злокачественная опухоль в течение среднего периода наблюдения 9,6 лет.
У детей сосудистые аномалии чаще встречаются вне мочевого пузыря, но чрезвычайно редко могут быть и в мочевом пузыре, и на сегодняшний день имеется лишь несколько сообщений о подобных случаях. Исследователи крупнейшей серии случаев, связанных с аномалиями мочеполовой системы и промежности у детей, проанализировали 3780 историй болезни пациентов за 5-летний период и обнаружили только 85 (2,2%) случаев, ни один из которых не был связан с мочевым пузырем.
В целом, сосудистые опухоли встречаются чаще, чем сосудистые мальформации, и описаны как врожденные, так и инфантильные гемангиомы. Эти опухоли обычно проявляются безболезненной рецидивирующей макроскопической гематурией; редко возникает гиповолемический шок, вызванный массивным кровотечением. Гистопатологически внешний вид гемангиом мочевого пузыря ничем не отличается от гемангиом, обнаруженных в других частях тела.
При УЗИ сосудистая опухоль может проявляться в виде полиповидного внутрипросветного солидного образования с повышенной васкуляризацией или реже в виде гиперемированного диффузного утолщения стенки мочевого пузыря, иногда содержащего точечные кальцификации. Опухоли чаще локализуются на куполе мочевого пузыря или на заднебоковых стенках и обычно одиночные. Множественные гемангиомы мочевого пузыря могут наблюдаться при синдроме
Клиппеля-Треноне-Вебера(Klippel-Tre
naunay-Weber) или Стерджа-Вебера(Sturge-Weber). Однако даже при отсутствии синдрома сосудистой мальформации кожные сосудистые мальформации можно увидеть в других частях тела примерно в 30% случаев.
Сосудистые опухоли обычно лечат абляцией опухоли; однако может потребоваться частичная или тотальная цистэктомия, если образование большое, с глубоким распространением и вызывает значительное кровотечение. Дифференциальный диагноз может включать остаточный абсцесс мочевого пузыря (если на куполе мочевого пузыря видно образование), цистит, рабдомиосаркому и даже гиперемированную грануляционную ткань из места предшествующей биопсии мочевого пузыря.
Другие сосудистые аномалии мочевого пузыря, наблюдаемые у детей, включают лимфатические и артериовенозные мальформации и телеангиэктазии стенки мочевого пузыря (на фоне атаксии-телеангиэктазии). Агрессивные и потенциально злокачественные сосудистые опухоли включают эпителиоидную гемангиоэндотелиому и ангиосаркому. Однако это чрезвычайно редкие опухоли.
Уротелиальные новообразования у детей встречаются редко и преимущественно неинвазивны. В серии случаев, включающих обзор уротелиальных опухолей мочевого пузыря у 23 пациентов моложе 20 лет, 10 (43,5%) случаев были связаны с PUNLMP; восемь (34,8%) с уротелиальными карциномами низкой степени злокачественности; и две (8,7%) с уротелиальными папилломами, три (13%) случая были связаны с уротелиальными карциномами высокой степени злокачественности. Различные подтипы уротелиальных новообразований мочевого пузыря невозможно отличить друг от друга при визуализации. Однако знание анамнеза пациента — например, истории хирургического вмешательства в анамнезе или синдрома, предрасполагающего к раку, — может сделать определенные подтипы уротелиального поражения более вероятными.
Хотя уротелиальные карциномы являются наиболее распространенными злокачественными новообразованиями мочевыводящих путей у взрослых, у детей они встречаются редко и имеют совершенно иное клиническое течение. Большинство этих опухолей имеют низкосортную морфологию и солитарны (в 94% случаев). Они связаны с низким риском рецидива и редко поражают верхние мочевые пути. Уротелиальные карциномы обычно выявляются у подростков; они встречаются у лиц в возрасте 10 лет и младше только в 30% случаев. При визуализации нет специфических признаков, отличающих уротелиальные карциномы от других уротелиальных опухолей мочевого пузыря; однако они имеют тенденцию возникать в области пузырного треугольника и устьев мочеточников.
Уротелиальная карцинома может возникать как вторичная первичная опухоль у молодых людей, перенесших ретинобластому, или на фоне других предрасполагающих к раку детей синдромов, таких как синдром Костелло(Costello) и синдром наследственного неполипозного колоректального рака. Пациенты с аугментационной цистопластикой в анамнезе имеют повышенный риск развития уротелиальной карциномы, которая в этих условиях чаще возникает в местах анастомоза мочевого пузыря и кишечника, чаще имеет высокую степень злокачественности и агрессивное клиническое течение. По этой причине некоторые клиницисты рекомендуют эндоскопическое наблюдение за пациентами с таким анамнезом. Это наблюдение должно начинаться через 10 лет после первоначальной операции из-за значительного времени, необходимого для развития опухоли.
Методом выбора лечения при уротелиальных карциномах низкой степени злокачественности является трансуретральная резекция; однако в некоторых (редких) случаях может потребоваться частичная цистэктомия. Не существует стандартного протокола динамического наблюдения за пролеченными пациентами, и сообщалось о рецидивах, особенно при изначальном наличии множественных опухолей. Хотя некоторые рекомендуют проводить регулярные УЗИ, частота этих обследований и продолжительность наблюдения являются спорными.
Папиллярное уротелиальное новообразование с низким злокачественным потенциалом
Папиллярное уротелиальное новообразование с низким злокачественным потенциалом (PUNLMP) — часто встречающаяся опухоль мочевого пузыря у детей. Из 140 опухолей мочевого пузыря в базе данных наблюдения, эпидемиологии и конечных результатов, которые были проанализированы с 1973 по 2003 год, 71 (50,7%) были PUNLMP. Термин папиллярное уротелиальное новообразование с низким злокачественным потенциалом был добавлен в систему классификации Всемирной организации здравоохранения и Международного общества урологической патологии 2004 г. для описания уротелиальной опухоли, которая напоминает экзофитную уротелиальную папиллому, но имеет повышенную клеточную пролиферацию, толщина которой превышает толщину нормального уротелия. До реклассификации эти опухоли были известны как уротелиальные карциномы 1 степени.
При визуализации PUNLMP трудно отличить от неинвазивной уротелиальной карциномы. Обычно они одиночные, размером 1–2 см и, по описанию, имеют вид «морских водорослей в океане». Они обычно возникают на задней боковой стенке и устьях мочеточников мочевого пузыря, неинвазивны и не метастазируют.
Сообщается, что примерно 35% PUNLMP рецидивируют после резекции, а 11% из них увеличиваются в размерах, если их не лечить; поэтому рекомендуется визуализирующее наблюдение. Время начала и продолжительность наблюдения не стандартизированы.
Уротелиальные папилломы представляют собой доброкачественные полипоидные уротелиальные новообразования, которые обычно наблюдаются у лиц мужского пола моложе 50 лет; о них редко сообщалось у детей. Микроскопически эти опухоли демонстрируют фиброваскулярное ядро, покрытое нормальным уротелием, без цитологической атипии. Иногда крупные папиллярные структуры могут отпочковываться, давая начало более мелким ветвям или анастомозам сосочков, что помогает отличить эти опухоли от фиброэпителиальных полипов при патоморфологическом анализе.
Уротелиальные папилломы были описаны как ветвеобразные при визуализации, хотя эта особенность не является патогномоничной, и возникают вблизи устьев мочеточников или вдоль задней стенки мочевого пузыря. Трансуретральное иссечение является методом выбора лечения. Из-за ограниченного опыта лечения этой редкой опухоли у детей варианты лечения остаются спорными. Поскольку известно, что уротелиальные папилломы, наблюдаемые у взрослых, рецидивируют, рекомендуется последующее наблюдение УЗИ. Опять же, нет стандартизированного временного интервала для этого последующего наблюдения ни в одном протоколе лечения.
Фиброэпителиальные полипы являются доброкачественными уротелиальными опухолями и чаще встречаются в верхних мочевых путях у взрослых. У детей они обычно возникают на шейке мочевого пузыря или рядом с ней. Они проявляются у детей со средним возрастом 9 лет, могут проявляться в младенчестве и имеют сильную предрасположенность к мужскому полу.
Проявления фиброэпителиальных полипов включают макрогематурию и боль в боку, что может быть связано с перекрутом полипа, если он достигает значительных размеров. Тем не менее, большинство этих опухолей одиночные и имеют размер менее 5 см. Микроскопически фиброэпителиальные полипы состоят из папиллярных ветвей, выстланных нормальным уротелием без клеточной атипии. Некоторые из них могут иметь очаговые участки изъязвления.
Нет никаких специфических радиологических признаков, которые отличают фиброэпителиальные полипы от других опухолей мочевого пузыря, и дифференциальный диагноз включает уротелиальные папилломы и рабдомиосаркомы ботриоидного типа.
Нейроэндокринные опухоли: Параганглиома
Феохромоцитомы вненадпочечникового происхождения известны как параганглиомы, а мочевой пузырь является наиболее частой локализацией мочеполовых параганглиом. Эти опухоли возникают из эмбриональных остатков хромаффинных клеток симпатического сплетения детрузора. Они чаще встречаются у взрослых в возрасте от 30 до 60 лет, но могут встречаться и у лиц в возрасте 10–88 лет. Мочеполовые параганглиомы встречаются крайне редко, составляя менее 0,5% всех опухолей мочевого пузыря у взрослых и детей вместе взятых.
Мочеполовые параганглиомы обычно доброкачественные, но 10% из них могут быть злокачественными, и они часто гормонально активны. Симптомы при манифестации связаны с избытком катехоламинов и обычно включают гипертензию и головную боль, которые могут быть связаны с мочеиспусканием.
Эти опухоли обычно интрамуральные и располагаются в боковой или задней стенке мочевого пузыря. На МРТ они обычно слегка гиперинтенсивны по сравнению с мышцами на Т1-взвешенных изображениях и гиперинтенсивны на Т2-взвешенных изображениях. Параганглиомы, как правило, представляют собой сосудистые опухоли, демонстрирующие активные характеристики усиления. Присутствие повышенной активности индикаторов на изображениях ядерной медицины, таких как ПЭТ-сканирование с йодом-131-метайодбензилгуанидином и фтор-18-фтордезоксиглюкозой, может быть полезным для подтверждения диагноза и выявления метастазов в лимфатических узлах. Хирургическое иссечение обычно приводит к излечению, хотя следует соблюдать осторожность, учитывая вероятность интраоперационного гипертонического криза.
Железистые опухоли мочевого пузыря: нефрогенная аденома
Нефрогенная аденома мочевого пузыря определяется как метапластическое изменение мочевого пузыря с папиллярными или скрытыми структурами, сходными с таковыми в почечных канальцах. Эти опухоли встречаются редко, на сегодняшний день зарегистрировано всего около 400 случаев, и примерно 10% случаев выявлено у детей. Как правило, в анамнезе имеется хирургическое вмешательство на мочеполовом тракте (примерно 10% пациентов перенесли трансплантацию почки) или лежащий в основе воспалительный или травматический процесс, такой как конкременты, травма, иммуносупрессия или цистит. В отличие от других образований мочевого пузыря, нефрогенные аденомы обычно проявляются частым мочеиспусканием, а не гематурией.
При макроскопическом анализе примерно половина этих новообразований выглядит как папиллярные опухоли, 35% из них выглядят как опухоль на широком основании, а 10% из них выглядят как полипы. Размеры этих опухолей значительно варьируют от микроскопических до более 4 см (в 10% случаев). Наибольшее зарегистрированное образование у ребенка имело размеры до 7 см. Особенности визуализации нефрогенных аденом аналогичны таковым при уротелиальных новообразованиях. Для лечения требуется удаление причинных факторов, если они известны (например, конкременты), и иссечение опухоли. Однако в случае диссеминированных полиповидных нефрогенных аденом у мальчика 12 лет успешное разрешение симптомов и поражений было достигнуто за счет регулярного внутрипузырного введения гиалуроната натрия каждые 2 недели в течение 5 месяцев.
Несколько потенциальных ловушек связаны с визуализацией мочевого пузыря у детей. Эти ловушки классифицированы и кратко описаны в следующих разделах, чтобы подчеркнуть важность соблюдения осторожности при визуализации малого таза, особенно при рассмотрении патологических состояний мочевого пузыря.
Образование малого таза ошибочно принятое за образование мочевого пузыря
Из-за анатомии малого таза воспалительные или злокачественные образования, возникающие из соседних структур, являются источником потенциальных ловушек, связанных с неправильной интерпретацией результатов визуализации. Эти неправильные интерпретации могут включать образования яичников, кишечника, костных структур или лимфатических узлов. Образования могут примыкать к мочевому пузырю и казаться возникающими из него, или они могут фактически возникать из мочевого пузыря, но быть ошибочно истолкованы как возникающие из соседней структуры. Парадоксально, но чем больше опухоль, тем сложнее определить место ее происхождения.
Если вы видите структуру в малом тазу и обнаруживаете, что она заполнена жидкостью, важно помнить несколько важных фактов и принять некоторые практические меры, прежде чем ставить диагноз. Во-первых, важно определить, можно ли увидеть нормальный мочевой пузырь отдельно от структуры. Нормальная стенка мочевого пузыря обычно имеет более эхогенный внутренний просветный слой и гипоэхогенный мышечный слой детрузора при УЗИ. Когда мочевой пузырь наполнен (на 90–100%), стенка мочевого пузыря может иметь толщину до 0,3 мм, тогда как киста может иметь тонкую эхогенную стенку. При наличии воспалительного образования стенка может быть толще.
Если трудно идентифицировать мочевой пузырь, может быть полезным повторное обследование пациента с пустым или наполненным мочевым пузырем, так как это позволяет увидеть, исчезает ли структура в малом тазу (при опорожненном мочевом пузыре) или визуализируется как отдельная структура при наполненном мочевом пузыре. Если установлен катетер, УЗИ можно повторить, заполняя мочевой пузырь подогретой стерильной водой непосредственно перед повторным исследованием или пережимая катетер не менее чем на 1 час перед повторным исследованием.
Нормальный вариант или складка стенки мочевого пузыря ошибочно интерпретируемая как образование
Из-за объемного воздействия на заднюю стенку мочевого пузыря или наличия дефекта наполнения при рентгеноскопии нормальный анатомический вариант, такой как большая матка (из-за удвоения матки, связанный с масс-эффектом) или уретероцеле (связанный с дефектом наполнения) может создаться впечатление наличия образования мочевого пузыря. Тщательная оценка с использованием УЗИ, обычно может помочь уточнить анатомию малого таза.
Воспалительное или неопухолевое образование, ошибочно истолкованное как опухоль
В редких случаях цистит имитирует новообразование мочевого пузыря, такое как рабдомиосаркома. Термины псевдотуморальный цистит, фолликулярный цистит, железистый цистит и буллезный цистит использовались в литературе для описания доброкачественных воспалительных массоподобных образований(*псевдоопухолей) стенки мочевого пузыря. Также описан ВК-вирус-ассоциированный геморрагический цистит, проявляющийся в виде сосудистых пристеночных узелков на фоне диффузного утолщения стенки мочевого пузыря у ребенка, перенесшего трансплантацию гемопоэтических стволовых клеток, который может симулировать образования мочевого пузыря. Подобные образования могут быть связаны с фокальными отечными изменениями в собственной пластинке или пролиферацией слизистых и подслизистых желез в эпителиальном слое, при этом образуются кистоподобные возвышения, которые имитируют полипоидный вид на изображениях.
Эозинофильный цистит является редким дифференциальным диагнозом, и он также может иметь вид опухоли на изображениях. Стенка мочевого пузыря может иметь выраженный гиперемированный вид при цветной допплерографии, могут быть клинические признаки макрогематурии. Моча обычно стерильна, в анамнезе может быть атопия. Опухолеподобный вид при этом состоянии, как полагают, связан с антигенным стимулом, который способствует опосредованному иммуноглобулином Е привлечению эозинофилов по всей стенке мочевого пузыря с последующей массовой дегрануляцией клеток с высвобождением медиаторов воспаления. Терапия, как правило, консервативная, и заболевание в основном самокупируется.
Врожденные рудименты мочевого пузыря, в частности кисты мочевого пузыря, обычно описываются как внешние по отношению к мочевому пузырю. Тем не менее, есть сообщения о случаях, когда эти кисты, расположенные в передне-верхней части мочевого пузыря, визуализировались как внутрипузырные образования, вдавливались в просвет мочевого пузыря или дренировались внутрипузырно. При инфицировании кисты урахуса могут иметь гиперваскулярную и гетерогенную эхоструктуру при УЗИ и иметь различное усиление при томографической визуализации. Следовательно, эти кисты могут быть легко ошибочно приняты за другие новообразования мочевого пузыря, такие как гемангиомы, рабдомиосаркомы или IMT. Опухоли, возникающие из рудиментов урахуса, редко возникают в детстве; однако, учитывая повышенный риск аденокарциномы, возникающей из этих рудиментов во взрослом возрасте, их обычно лечат хирургическим путем, когда они обнаруживаются случайно.
Для неподготовленного глаза утолщенный мочевой пузырь у новорожденных с клапанами задней уретры на УЗИ также может быть похожим на объемное образование. Однако это патологическое образование встречается гораздо чаще, чем образования мочевого пузыря новорожденных. Типичные признаки расширенной задней уретры и трабекулярного мочевого пузыря небольшого объема при последующей миктурирующей цистоуретрографии помогают подтвердить диагноз.
Подвижный или ятрогенный материал в мочевом пузыре ошибочно интерпретируемый как опухоль
Подвижный материал мочевого пузыря может включать конкременты мочевого пузыря, слоистую взвесь и/или гематому. Эти патологические образования должны демонстрировать некоторую подвижность при повороте пациента на бок и при повторной визуализации; таким образом, важно определить, действительно ли опухоль мочевого пузыря фиксирована к стенке мочевого пузыря. Гематомы могут быть связаны с известными фоновыми патологическими состояниями и методами лечения, такими как геморрагический цистит и прием антикоагулянтов соответственно. Они не имеют внутреннего кровотока при цветном доплеровском УЗИ и могут демонстрировать уменьшение в размере при последующей визуализации. В последние годы возросла всемирная популярность сополимера декстраномера и гиалуроновой кислоты (Deflux; Salix Pharmaceuticals, Бриджуотер, Нью-Джерси), который эндоскопически вводят в подмочеточниковое пространство в качестве минимально инвазивного лечения пузырно-мочеточникового рефлюкса. Обызвествление этого ятрогенного материала является распространенным явлением и может быть неверно истолковано как конкремент дистального отдела мочеточника или мочевого пузыря или объемное образование при визуализации. Это образование не становится подвижным при изменении положения пациента и является эхогенным на изображениях УЗИ. На КТ отличительными признаками инъецированного сополимера декстраномера и гиалуроновой кислоты, включают отсутствие ассоциированной дилатации мочеточника и значение затухания ниже 400 HU. В одном исследовании сополимера декстраномера и гиалуроновой кислоты с участием 16 детей, которые прошли визуализацию через 1–40 месяцев после процедуры инъекции, этот материал имел повышенную интенсивность сигнала на Т2-взвешенных МР-изображениях, но не был идентифицирован ни с какими другими последовательностями МР-изображений, включая МРТ с гадолинием. В целом, если эхогенное образование наблюдается вблизи устья мочеточника или дистального отдела мочеточника, отсутствие клинических симптомов почечной колики в сочетании с информацией о недавней урологической процедуре по поводу рефлюкса должно насторожить радиолога о потенциальном наличии этого феномена.
По сравнению с новообразованиями мочевого пузыря у взрослых новообразования мочевого пузыря у детей встречаются редко и имеют другой гистологический спектр. Большинство этих образований доброкачественные. Наиболее частой злокачественной опухолью мочеполового тракта у детей является рабдомиосаркома, за которой следуют уротелиальные опухоли. Сообщается, что PUNLMP являются наиболее распространенными уротелиальными опухолями в педиатрической популяции. Первоначальное визуализирующее обследование должно включать УЗИ, желательно при наполненном мочевом пузыре пациента.
Из-за анатомии малого таза воспалительные или злокачественные образования, возникающие из соседних структур, являются источником потенциальных ловушек неправильной интерпретации при визуализации. Эти неправильные интерпретации могут включать образования яичников, прямой кишки, костных структур или лимфатических узлов. Кроме того, некоторые неопухолевые образования мочевого пузыря, такие как связанное с циститом утолщение стенки мочевого пузыря и конкременты в мочевом пузыре, могут быть похожими на новообразования и ошибочно интерпретироваться как опухоли. Знание этих подводных камней необходимо для того, чтобы избежать диагностических дилемм.
*Также в публикации присутствуют эхограммы, интраоперационные снимки, а также МРТ.
*комментарии редактора